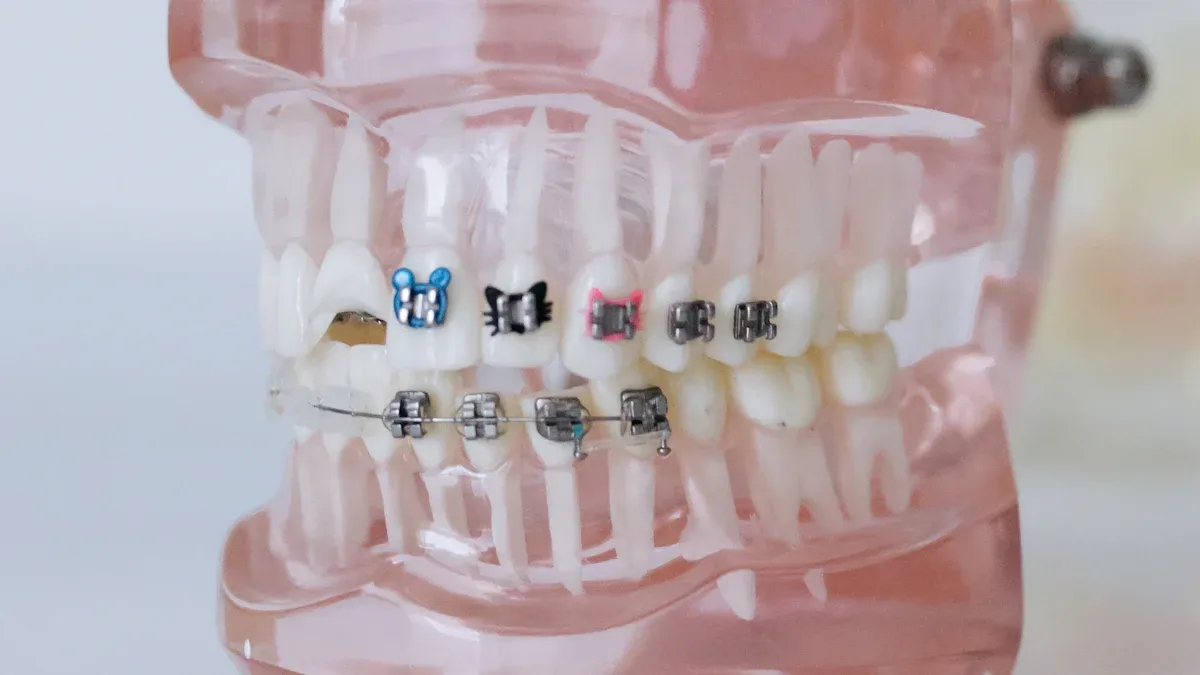
ISO 13485, FDA 21 CFR Part 820 ja CE-merkintä (MDR) eivät ole neuvoteltavissa seuraaville tuotteille.hammaslääketieteelliset oikomishoidon instrumentittoimittajat vuonna 2025. Nämä sertifikaatit varmistavat tuotteen laadun, potilasturvallisuuden ja markkinoille pääsyn. HyvämaineinenISO 13485 -sertifioitu oikomishoidon instrumenttien toimittaja, kutenDenrotary-lääketieteellinen laite, priorisoi näitä kriittisiä standardeja. Ne takaavat esimerkiksi seuraavien tuotteiden luotettavuuden:Autoklavoitavat oikomishoidon pihdit vientiinja muutKirurgiset ruostumattomasta teräksestä valmistetut instrumentitMyös muut keskeiset sertifikaatit ovat edelleen olennaisia kaikille hammasoikomishoidon instrumenteille.
Keskeiset tiedot
- ISO 13485, FDA 21 CFR Part 820 ja CE-merkintä ovat erittäin tärkeitä hammashoidon työkaluille. Ne varmistavat, että työkalut ovat turvallisia ja toimivat hyvin.
- MDSAP auttaa työkaluvalmistajia saamaan hyväksynnän useissa maissa vain yhdellä tarkastuksella. Tämä nopeuttaa työkalujen myyntiä ympäri maailmaa.
- ISO 14971 auttaa yrityksiä löytämään ja korjaamaan hammashoitolaitteiden ongelmia. Tämä pitää potilaat turvassa työkaluja käyttäessään.
- Kyberturvallisuussäännöt suojaavat tietokoneisiin kytkettäviä älykkäitä hammashoitolaitteita. Ne pitävät potilastiedot yksityisinä ja turvassa hakkereilta.
- Tarkista aina toimittajan sertifikaatit. Näin varmistat, että ostat potilaillesi hyviä ja turvallisia hammashoitovälineitä.
Hammaslääketieteellisten oikomishoidon instrumenttien perustavanlaatuinen laadunhallinta

ISO 13485:2016 – Lääkinnällisten laitteiden laatujärjestelmät
ISO 13485:2016 tarjoaamaailmanlaajuisesti tunnustettu viitekehyslääkinnällisten laitteiden teollisuuden laadunhallintajärjestelmille.Tämä sertifikaattion ratkaisevan tärkeää hammaslääketieteellisten oikomishoidon instrumenttien toimittajille. Se varmistaakansainvälisten turvallisuus- ja laatustandardien noudattaminenValmistajat hyötyvät parantuneesta potilasturvallisuudesta ja tehokkuudesta. He saavat myös pääsyn uusille markkinoille. Monet maat ovat jopa tehneet tästä sertifioinnista pakollisen.
ISO 13485 -standardin vuoden 2016 versio toi mukanaan merkittäviä päivityksiä. Se asettaasuurempi painotus riskienhallintaanTämä lähestymistapa auttaa ennakoimaan mahdollisia ongelmia. Standardi on myös paremmin linjassa FDA:n 21 CFR Part 820:n kanssa. Keskeisiin muutoksiin kuuluvat uudet vaatimuksetdokumenttien hallinta ja johdon tarkastusSe käsittelee myös henkilöstöresursseja ja infrastruktuuria. Standardi edellyttää riskiperusteista lähestymistapaa kaikissa laatujärjestelmän prosesseissa. Tämä ulottuu pelkän tuoteriskin ulkopuolelle. Lisäksi se edellyttää laadunhallintajärjestelmässä käytettyjen tietokoneohjelmistojen validointia.
FDA 21 CFR Osa 820 – Hammaslääketieteellisten oikomishoidon instrumenttien laatujärjestelmäasetus (QSR)
FDA 21 CFR Part 820, joka tunnetaan nimellä Quality System Regulation (QSR), on olennainen Yhdysvalloissa tuotteita myyville lääkinnällisten laitteiden valmistajille. Tämä asetus asettaa vaatimukset laadunhallintajärjestelmille. Se varmistaa, että lääkinnälliset laitteet ovat turvallisia ja tehokkaita. QSR kattaa laitteen suunnittelun, valmistuksen, pakkaamisen, merkinnän, varastoinnin ja asennuksen eri osa-alueet.
Tämän asetuksen keskeisiin osiin kuuluvat erityisvaatimukset asiakirjoille. Esimerkiksi § 820.180 esittää yleiset vaatimukset asiakirjojen ylläpidolle. Toinen tärkeä osio, § 820.198, määrittelee valitustiedostojen asianmukaisen käsittelyn ja ylläpidon. Päivitetty ISO 13485:2016 -standardi on entistä yhdenmukaisempi FDA 21 CFR Part 820:n kanssa. Tämä sisältäätarkennetut suunnittelun valvonnan vaatimukset ja uudet menettelyt, kuten johdon katselmusValmistajien on noudatettava näitä määräyksiä varmistaakseen tuotteiden laadun ja potilasturvallisuuden.
Markkinoille pääsy ja tuotekohtaiset sertifioinnit hammaslääketieteellisille oikomishoidon instrumenteille
Valmistajien on hankittava tietyt sertifikaatit päästäkseen globaaleille markkinoille. Nämä sertifikaatit osoittavat alueellisten määräysten noudattamisen. Ne takaavat myös tuoteturvallisuuden ja suorituskyvyn.
CE-merkintä (EU:n lääkinnällisiä laitteita koskeva asetus – MDR 2017/745)
CE-merkintä on pakollinen vaatimustenmukaisuusmerkintä Euroopan talousalueella (ETA) myytäville tuotteille. Lääkinnällisten laitteiden osalta tätä prosessia säätelee EU:n lääkinnällisiä laitteita koskeva asetus (MDR 2017/745). Tämä asetus korvasi vanhemman lääkinnällisiä laitteita koskevan direktiivin (MDD). Se otti käyttöön tiukemmat vaatimukset valmistajille. MDR korostaa potilasturvallisuutta ja tuotteiden suorituskykyä. Se vaatii vankempaa kliinistä näyttöä ja markkinoille saattamisen jälkeistä valvontaa.Valmistajien on esiteltävä tuotteensatäyttävät nämä tiukat standardit. Tämä varmistaa, että hammaslääketieteelliset oikomishoidon instrumentit ovat turvallisia ja tehokkaita käyttää kaikkialla Euroopassa.
MDSAP (lääkinnällisten laitteiden yhden auditoinnin ohjelma) hammaslääketieteellisille oikomishoidon instrumenteille
Lääkinnällisten laitteiden yhtenäinen tarkastusohjelma (MDSAP) tarjoaa virtaviivaisen lähestymistavan määräystenmukaisuuteen. Sen avulla yksi tarkastus voi täyttää useiden sääntelyviranomaisten vaatimukset. Tämä ohjelma tarjoaa merkittäviä etuja valmistajille. Valmistajat voivat välttää erillisten tarkastusten tekemisen kullekin maalle, mikä virtaviivaistaa vaatimustenmukaisuusprosessia. Tämä johtaa myös nopeampiin viranomaishyväksyntöihin. Sertifiointi voi nopeuttaa markkinoille pääsyä osallistuvilla alueilla. Se myös parantaa uskottavuutta. MDSAP rakentaa luottamusta monikansallisten jakelijoiden ja hankintapäälliköiden kanssa. Se viestii valmiudesta monimutkaisiin kansainvälisiin kumppanuuksiin. MDSAP toimii kansainvälisen kaupan "passina". Se helpottaa sujuvampaa jakelua ja laillista hyväksyntää säännellyillä markkinoilla.1. tammikuuta 2019 alkaen Health Canada vaatii yksinomaan MDSAP-sertifioinnin.lääkinnällisten laitteiden valmistajille. Yhdysvaltain elintarvike- ja lääkevirasto (USFDA), Kanadan terveysvirasto (Health Canada), Brasilian ANVISA, Japanin MHLW ja Australian Therapeutic Goods Administration hyväksyvät kaikki MDSAP-auditointiraportit.
Hammaslääketieteellisten oikomishoidon instrumenttien erikoistuneet ja uudet sertifioinnit vuonna 2025
ISO 14971 – Hammaslääketieteellisten oikomishoidon instrumenttien riskienhallinta
ISO 14971 tarjoaa viitekehyksen lääkinnällisten laitteiden riskienhallinnalle. Tämä standardi auttaa valmistajia tunnistamaan, arvioimaan, hallitsemaan ja seuraamaan tuotteisiinsa liittyviä riskejä. Se varmistaa potilasturvallisuuden koko tuotteen elinkaaren ajan.hammaslääketieteelliset oikomishoidon instrumentitTämä tarkoittaa materiaalien, suunnitteluvirheiden, valmistusprosessien ja kliinisen käytön mahdollisten riskien arviointia. Valmistajat soveltavat systemaattista lähestymistapaa mahdollisten haittojen minimoimiseksi. Tämä ennakoiva riskienhallinta on ratkaisevan tärkeää turvallisten ja tehokkaiden instrumenttien kehittämisen kannalta.
Verkkoon kytkettyjen hammaslääketieteellisten oikomishoidon instrumenttien kyberturvallisuussertifikaatit
Nykyaikaiset hammaslääkäriasemat käyttävät yhä enemmän verkotettuja laitteita. Nämä laitteet yhdistyvät potilastietoihin, kuvantamisjärjestelmiin ja muihin digitaalisiin alustoihin. Kyberturvallisuussertifikaatit suojaavat arkaluonteisia potilastietoja ja varmistavat näiden laitteiden luotettavan toiminnan. Ne puuttuvat uhkiin, kuten tietomurtoihin, luvattomaan käyttöön ja järjestelmän toimintahäiriöihin. Yhä useammathammaslääketieteelliset oikomishoidon instrumentitdigitaalisesti integroituvat, NIST-ohjeisiin tai IEC 80001-1 -standardiin perustuvat sertifioinnit ovat elintärkeitä. Ne varmistavat sekä laitteen että sen käsittelemien potilastietojen turvallisuuden ja eheyden.
Hammaslääketieteellisten oikomishoidon instrumenttien ympäristö- ja kestävyyssertifikaatit
Ympäristövastuu on kasvava huolenaihe kaikilla toimialoilla, myös lääkinnällisten laitteiden valmistuksessa. Valmistajat ottavat nyt huomioon ekologisen jalanjälkensä. Kestävän kehityksen sertifioinnit vastaavat näihin huolenaiheisiin. Hammaslääketieteellisten oikomishoidon instrumenttien valmistus luomerkittävää muovijätettäTämä sisältää oikomislaitteet, 3D-mallit ja pakkausmateriaalit. Hävitysongelmia syntyy, koska monilla oikomislaitteilla ei ole tehokkaita kierrätysprosesseja. Tuotantoprosessiin liittyy myös luontainen resurssien kulutus. Sertifioinnit kannustavat ympäristöystävällisiin materiaaleihin ja prosesseihin. Ne edistävät vastuullista jätteenkäsittelyä ja energiankulutuksen vähentämistä. Nämä sertifikaatit osoittavat sitoutumista ympäristönsuojeluun.
Hammaslääketieteellisten oikomishoidon instrumenttien toimittajien sertifiointien varmentaminen
Toimittajien sertifiointien varmistaminen on ratkaiseva vaihe. Se varmistaa ostamiesi tuotteiden laadun ja vaatimustenmukaisuuden. Tämä prosessi suojaa vastaanottoasi ja potilaitasi. Voit käyttää useita menetelmiä toimittajan väitteiden vahvistamiseen.
Julkiset tietokannat ja rekisterit sertifiointien validointia varten
Monet sääntelyelimet ylläpitävät julkisia tietokantoja. Näiden resurssien avulla voit varmistaa toimittajan sertifiointitilan. Esimerkiksi FDA:n verkkosivustolla on luettelo rekisteröidyistä lääkinnällisten laitteiden laitoksista. Voit hakea valmistajia ja heidän tuoteluetteloitaan. Vastaavasti Euroopan komission NANDO-tietokanta tarjoaa tietoa ilmoitetuista laitoksista. Nämä laitokset myöntävät CE-merkintätodistuksia. Voit tarkistaa CE-sertifikaatin voimassaolon ja laajuuden tämän järjestelmän kautta. ISO-sertifiointielimillä on usein myös online-hakemistoja. Näiden hakemistojen avulla voit tarkistaa, onko yrityksellä voimassa oleva ISO 13485 -sertifiointi. Vertaile aina toimittajan verkkosivustolla olevia tietoja näihin virallisiin lähteisiin. Tämä vaihe auttaa estämään harhaanjohtamista.
Toimittajien dokumentaatio ja auditointiraportit
Toimittajalta suoraan pyydettävät asiakirjat ovat toinen olennainen varmennusmenetelmä. Pyydä kopioita heidän todellisista sertifikaateistaan. Näissä asiakirjoissa tulee selvästi mainita sertifiointilaitos, standardi (esim. ISO 13485:2016) ja voimassaolopäivä. Tarkista myös sertifioinnin laajuus. Sen tulisi erityisesti kattaa lääkinnällisten laitteiden tai tarkemmin sanottuna hammaslääketieteellisten oikomishoidon instrumenttien valmistus. Auditointiraporttien pyytäminen voi antaa syvempää tietoa. Nämä raportit kuvaavat sertifiointiauditointien tuloksia yksityiskohtaisesti. Ne osoittavat, kuinka hyvin toimittajan laatujärjestelmä toimii. Hyvämaineinen toimittaja toimittaa nämä asiakirjat mielellään. He osoittavat läpinäkyvyyttä ja sitoutumista laatuun. Varmista aina, että asiakirjat ovat ajan tasalla ja relevantteja tuotteille, joita aiot ostaa.
ISO 13485-, FDA 21 CFR Part 820- ja CE-merkinnällä (MDR) varustettujen toimittajien priorisointi on ensiarvoisen tärkeää hammaslääketieteellisille oikomishoidon instrumenteille. Nämä sertifikaatit tarjoavat perustavanlaatuiset takeet laadusta, turvallisuudesta ja määräystenmukaisuudesta. Ne suojaavat potilaita ja parantavat vastaanoton tuloksia. Näiden sertifikaattien huolellinen tarkistaminen turvaa potilaiden hyvinvoinnin. Se myös parantaa vastaanoton onnistumista. Varmista aina nämä standardit...luotettavia tuotteita. ✅
Usein kysytyt kysymykset
Mitkä ovat tärkeimmät sertifioinnit hammaslääketieteellisille oikomishoidon instrumenteille?
ISO 13485, FDA 21 CFR Part 820 ja CE-merkintä (MDR) ovat ratkaisevan tärkeitä. Nämä sertifikaatit varmistavat tuotteen laadun, potilasturvallisuuden ja markkinoille pääsyn. Ne osoittavat toimittajan sitoutumisen kansainvälisiin standardeihin ja määräysten noudattamiseen.
Miten MDSAP auttaa hammaslääketieteellisten oikomishoidon instrumenttien valmistajia?
MDSAP mahdollistaa yhden auditoinnin, joka tyydyttää useiden sääntelyviranomaisten vaatimukset. Tämä tehostaa vaatimustenmukaisuutta, vähentää auditointitaakkaa ja nopeuttaa markkinoille pääsyä osallistujamaissa. Se myös parantaa uskottavuutta kansainvälisten kumppaneiden keskuudessa.
Miksi ISO 14971 on ratkaisevan tärkeä hammaslääketieteellisille oikomishoidon instrumenteille?
ISO 14971 tarjoaa riskienhallinnan viitekehyksen. Se auttaa valmistajia tunnistamaan, arvioimaan ja hallitsemaan tuotteisiinsa liittyviä riskejä. Tämä varmistaa potilasturvallisuuden koko laitteen elinkaaren ajan suunnittelusta kliiniseen käyttöön.
Milloin hammaslääketieteelliset oikomishoidon instrumentit tarvitsevat kyberturvallisuussertifikaatit?
Kyberturvallisuussertifikaatit ovat välttämättömiä verkotetuille hammasoikomishoidon instrumenteille. Nämä laitteet yhdistyvät digitaalisiin järjestelmiin ja käsittelevät arkaluonteisia potilastietoja. Sertifikaatit suojaavat tietomurroilta ja varmistavat luotettavan toiminnan turvaten sekä tiedot että laitteen eheyden.
Julkaisun aika: 04.12.2025


